Blog - Boletín Informativo RedLAM #9


Histórico aporte de la sociedad civil en Argentina: el INPI rechazó la patente de dos medicamentos esenciales para el VIH/SIDA
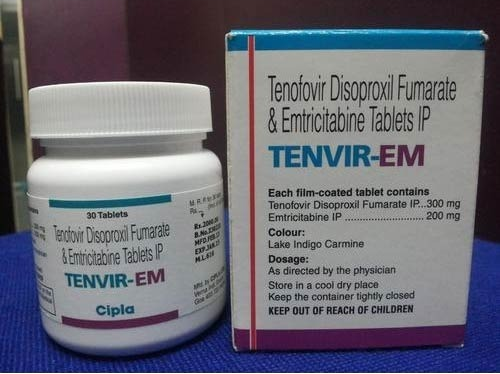
En dos decisiones que representan un avance en el resguardo del derecho a la salud el Instituto Nacional de la Propiedad Industrial (INPI) argentino desestimó la solicitud de patente para el medicamento antirretroviral tenofovir-emtricitabina (TDF-FTC, conocido por su nombre comercial Truvada®) presentada por la compañía farmacéutica multinacional Gilead y rechazó dos solicitudes de patente que la empresa AbbVie pretendía sobre la combinación de lopinavir/ritonavir (nombre comercial Kaletra®). Ambas decisiones se dieron a conocer entre mayo y junio pasados.
La Fundación GEP participó en el primer expediente mediante la presentación de una oposición a la patente en abril de 2015, remarcando que la solicitud no cumpe con los requisitos legales para que la patente sea concedida. Las pruebas presentadas por GEP forman parte de la justificación de los examinadores del INPI para la desestimación de la solicitud de Gilead, que en sus palabras “no se adecúa a los requisitos legales y reglamentarios” para merecer una patente. Asimismo, GEP aportó argumentos decisivos al segundo expediente en 2015 a través de otra oposición a la patente, probando que también en este caso las solicitudes incumplían los requisitos legales básicos y sólo buscaban extender ilegítimamente el monopolio de AbbVie sobre el medicamento hasta 2025.
La Comisión de Salud del Congreso de Perú declara de interés público el medicamento Atazanavir
De acuerdo a las organizaciones de la sociedad civil peruana que trabajan para favorecer el acceso al antirretroviral atazanavir, la decisión tomada por los legisladores el 24 de mayo es un gran avance en tanto representa un paso previo requerido para la emisión de una licencia obligatoria que permita el ingreso de competencia al mercado y la existencia de versiones genéricas asequibles que no comprometan la sustentabilidad de los programas de salud.Se espera que en último termino la medida permita:
– Romper el monopolio de Bristor Myers Squibb sobre su producto REYATAZ, que ha costado al Estado Peruano más de S/.75 millones de sobregasto en los últimos cuatro años.
– La Licencia Obligatoria, medida que los parlamentarios ven con optimismo, frente al abusivo precio del medicamento atazanavir.
– Que instituciones públicas y gremios como la Defensoría del Pueblo, el Ministerio de Salud, el Ministerio de Relaciones Exteriores, Colegios Profesionales Farmacéutico y Medica den opinión favorable.

|
||||||||||||||
|






